Ojo de Markov número setenta y uno - marzo 2018
22/03/2018
El aumento de la resistencia a los antimicrobianos constituye actualmente una grave amenaza para la salud.A
escala mundial, se considera que 700.000 personas mueren cada año por
infecciones resistentes a los antibióticos. Si no se hace nada, se prevé
que causen anualmente millones de muertes; para 2050, la resistencia a
los antimicrobianos podría convertirse en una causa de muerte más común
que el cáncer.
El problema deriva del mal uso de
los antibióticos en medicina, del abuso de ellos en veterinaria y de las
malas condiciones de higiene en centros sanitarios o en la cadena
alimentaria. Otro factor que influye es la falta de innovación en el
sector. La investigación de medicamentos recae principalmente en las
compañías farmacéuticas, las cuales buscan un retorno económico. Tal y
como está planteado el sistema, la industria invierte,
principalmente, en la investigación de aquello que le resulta más
rentable (como los fármacos para el tratamiento de enfermedades
crónicas); y los antibióticos, que son un tratamiento de corta duración,
no son su prioridad. Además, debido al problema de la
multirresistencia, los antibióticos nuevos deben reservarse solo para
cuando no hay alternativas o estas han fracasado, lo cual reduce más aún
su cuota de mercado.
Ante esta crisis global de falta
de antimicrobianos, es urgente actuar de forma coordinada e idear
fórmulas para incentivar la investigación a nivel mundial. En 2012, la
Unión Europea, en el marco de la Iniciativa sobre Medicamentos
Innovadores (IMI), puso en marcha la mayor asociación público-privada
del mundo, el programa New DrugsforBad Bugs
(ND4BB), dotado con un presupuesto global de unos 700 millones de
euros. En él confluyen académicos, otros socios públicos y empresas
farmacéuticas para impulsar la invención de nuevos antibióticos. En
junio de 2017, la Comisión Europea adoptó el nuevo plan de acción sobre resistencia a los antimicrobianos, siendo
la investigación de nuevos antibióticos uno de sus pilares. Por otro
lado, la OMS en su deseo de guiar y promover la investigación y
desarrollo (I+D) de nuevos antibióticos, en febrero de 2017 publicó la primera lista de «patógenos prioritarios»
resistentes a los antibióticos. En este listado se incluyen las 12
familias de bacterias más peligrosas para la salud humana. Considera
como prioridad crítica: Acinetobacterbaumannii, Pseudomonas aeruginosa y Enterobacteriaceae por su resistencia a carbapenemes (ver entrada en este Portal).
En la actualidad, las infecciones causadas por enterobacterias y Pseudomonas aeruginosa multirresistentes
productoras de betalactamasas de espectro extendido o de
carbapenemasas, constituyen un grave problema de salud. Las opciones
terapéuticas eficaces frente a estos patógenos son muy limitadas.
Recientemente han sido autorizados en España dos nuevos antibióticos,
ceftazidima-avibactam y ceftolozano-tazobactam, con perfiles de
sensibilidad prometedores. El desarrollo de resistencias a estos nuevos
antibióticos es una preocupación, por lo que algunos expertos
consideran que lo más prudente es reservarlos para los casos complicados
y pacientes de mayor riesgo (Rodriguez-Baño, et al. 2018).
A continuación, se resumen las
características de estos nuevos antibióticos y se analizan sus ventajas y
limitaciones de acuerdo a los resultados de los ensayos clínicos.
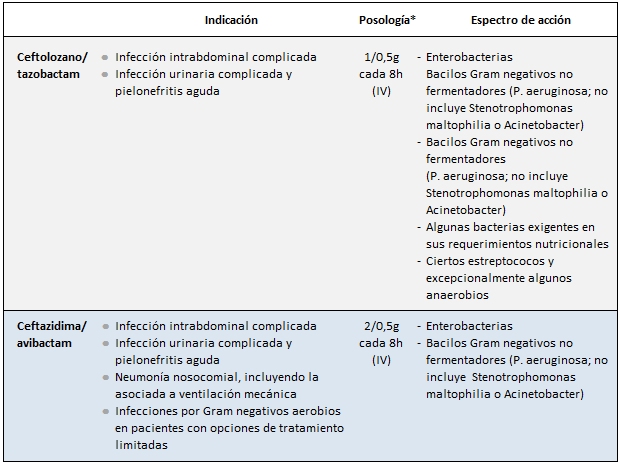
* En pacientes con insuficiencia renal ajustar la dosis según se indica en las fichas técnicas (Zerbaxa® y Zavicefta®)
Betalactamasas inhibidas potencialmente por estos antibióticos

* Ya se han descrito resistencias a ceftazidima/avibactam de cepas de Klebsiella pneumoniae productoras de carbapenemasas KPC (Shields, et al. AntimicrobAgentsChemother. 2017 Mar; 61).
Ceftolozano/tazobactam
1. Infección intrabdominal complicada (IIAc)
Ceftolozano/tazobactam (1/0,5g
cada 8h) asociado a metronidazol (500mg cada 8h) ha demostrado eficacia
en términos de no inferioridad frente a meropenem (1 g cada 8h), tanto
para la variable principal como para las secundarias (estudio ASPECT-cIAI).
Limitaciones
La población incluida
en el estudio contempla demasiados pacientes con foco primario de
infección de apéndice (≈50%); la guía de la EMA recomienda un máximo de
30%. En general, los pacientes incluidos presentan poca gravedad
(puntuaciones de APACHE bajas y mejoría con pocos días de tratamiento).
La eficacia no ha
quedado demostrada en los siguientes subgrupos de pacientes: graves
(APACHE>10), mayores de 65 años, con insuficiencia renal y con
infección en una localización distinta al apéndice. En estos subgrupos
la tasa de curación de ceftalozano/tazobactam fue inferior a la obtenida
con meropenem.
2. Infección urinaria complicada (ITUc)
Ceftolozano/tazobactam (1/0,5g
cada 8h) ha demostrado eficacia en términos de no inferioridad frente a
levofloxacino (750 mg cada 24 h), principalmente en pacientes con
pielonefritis (estudio ASPECT-cUTI).
Limitaciones
-
Inadecuado comparador: según las pruebas de sensibilidad del estudio, un 30% de las bacterias gram negativas y un 57% de las gram positivas eran resistentes a levofloxacino, lo que introduce un claro sesgo en los resultados.
-
La mayoría de los pacientes incluidos presentan pielonefritis (80%), lo que supone que la demostración de eficacia en otras ITUc se basa en tan solo 60 vs 66 pacientes por brazo. La EMA sugiere que ITUc y pielonefritis deben estudiarse por separado y, de no ser así, el porcentaje de pacientes con pielonefritis debe limitarse.
-
En pacientes con ITUc y sensibles a levofloxacino la no inferioridad de ceftolozano/tazobactam no ha sido demostrada.
-
Escaso número de infecciones causadas por bacterias productoras de BLEE, lo que limita las conclusiones de eficacia en estos microrganismos.
-
En pacientes con insuficiencia renal grave, alteración frecuente en este tipo de infecciones, se desconoce la dosis adecuada y seguridad de este fármaco ya que fueron excluidos del ensayo.
-
Baja representación de pacientes >65 años.
Bacteriemias
La experiencia de
ceftolozano/tazobactam en pacientes con bacteriemia se reduce a un
número pequeño de casos, por lo que los datos sobre su eficacia son
limitados para extraer conclusiones.
Neumonía nosocomial
En esta indicación
ceftolozano/tazobactam no está autorizado. Se está realizando un ensayo
clínico fase III con dosis dobles a las utilizadas en las anteriores
indicaciones, pero todavía no se conocen los resultados.
Seguridad
El perfil de seguridad de
ceftolozano/tazobactam ha resultado aceptable y similar al de los
comparadores en los diferentes ensayos clínicos.

Bibliografía consultada: Informe de evaluación de la EMA; Informe de posicionamiento terapéutico; estudio ASPECT-cIAI; estudio CENIT; estudio ASPECT-cUTI; evaluación crítica (Therapeutics and ClinicalRisk Management 2016).
Ceftazidima/avibactam
1. Infección intrabdominal complicada
Ceftazidima/avibactam (2/0,5g cada
8 h) en combinación con metronidazol (500mg cada 8h) ha demostrado la
no inferioridad frente a meropenem (1g cada 8h) -estudio RECLAIM I, II y III-.
En pacientes más graves (APACHE II>10) las tasa de curación del
grupo de ceftazidima/avibactam fue inferior a la obtenida con meropenem.
Limitaciones
- El porcentaje de infecciones debidas a perforación de apéndice supera el 30% recomendado por la EMA. La gravedad de las infecciones fue baja (APACHE<10 en el 80% de los casos).
- Pacientes con insuficiencia renal mostraron resultados inconsistentes. La tasa de curación en esta población fue inferior para ceftazidima/avibactam que para el comparador meropenem. Se ha postulado que podría deberse a infradosificación de ceftazidima/avibactam, por lo que la dosis recomendada en ficha técnica es más alta que la usada en los ensayos. Existe cierta incertidumbre sobre la dosis en pacientes con insuficiencia renal.
- La eficacia en pacientes graves (APACHE II>10) es inferior a la del comparador.
- No se pueden extraer conclusiones de eficacia para patógenos con resistencias producidas por carbapenemasas, ya que estas cepas apenas estuvieron representadas. La mayoría de patógenos resistentes a ceftazidima fueron productores de BLEE (en torno 80%).
2. Infección urinaria complicada
Ceftazidima/avibactam (2/0,5g cada
8 h) ha demostrado eficacia en términos de no inferioridad frente a
doripenem (500mg cada 8h) (estudio RECAPTURE).
Limitaciones
- Inadecuado comparador para nuestro ámbito, doripenem fue retirado por razones de seguridad.
- Bajo número de pacientes con ITUc; la mayoría de pacientes incluidos presentan pielonefritis (72%).
- La prevalencia de infecciones causadas por bacterias productoras de BLEE fue del 19%. Sobre otro tipo de resistencias no hay datos documentados.
3. Neumonía nosocomial y neumonía asociada a ventilación mecánica
Ceftazidima/avibactam ha demostrado eficacia en términos de no inferioridad frente a meropenem (estudio REPROVE, Lancet, dic 2017).
Limitaciones
- No se pueden extraer conclusiones de eficacia para patógenos con resistencias producidas por carbapenemasas. Se consideró criterio de exclusión pacientes en los que el patógeno aislado al principio no fuera susceptible de responder a alguno de los brazos de tratamiento.
- En pacientes con insuficiencia renal moderada y grave no se puede concluir eficacia. Tras el fracaso de curación obtenido en esta población en el estudio RECLAIM, en el que ceftazidima-avibactam fue administrado cada 12h, el protocolo del estudio REPROVE fue modificado. Los pacientes con insuficiencia renal moderada y grave que inicialmente recibieron la dosis cada 12h fueron excluidos del análisis.
- No se ha comparado con regímenes de meropenem distintos a 1 g/8h, es decir infusiones prolongadas o continuas.
4. Infecciones causadas por gram negativos en pacientes con opciones limitadas
Esta indicación se apoya en los
datos microbiológicos, ya que avibactam inhibe algunas carbapenemasas,
BLEE y enzimas AmpC, por lo que es esperable que la combinación con
ceftazidima sea de utilidad para el tratamiento de infecciones causadas
por gram negativos que se encuentren dentro del espectro de actividad de
ceftazidima. No se dispone de ensayos clínicos que apoyen esta
indicación.
Bacteriemias
En todos los ensayos el número de pacientes incluidos con bacteriemia es muy reducido para extraer conclusiones.
Seguridad
En el estudio REPROVE la tasa de
eventos adversos graves fue superior en el brazo de
ceftazidima/avibactam a la obtenida con meropenem (19% vs 13%). En estos
eventos adversos graves se incluyó muerte (no incluye la muerte por
progresión), amenaza para la vida, prolongación de la estancia
hospitalaria, etc.

Bibliografía consultada: Informe de evaluación de la EMA; Informe de posicionamiento terapéutico; estudio RECLAIM I, II y III; estudio RECAPTURE; estudio REPROVE.
Conclusiones
- El aumento de los microorganismos multirresistentes se ha convertido en un problema de salud púbica.
- Los nuevos antibióticos deben ser reservados y antes de utilizarlos valorar otras alternativas.
- La estrategia terapéutica debe individualizarse de acuerdo con la sensibilidad antibiótica, la gravedad de la infección y las características del paciente. En este sentido, es recomendable consultar a los equipos PROA de cada centro para que asesoren sobre el manejo terapéutico de este tipo de infecciones tan complejas.
Autora: Belén Calabozo Freile
Revisores: Julio Valdueza Beneitez y Jorge Elízaga Corrales
No hay comentarios:
Publicar un comentario